
医脉通:目前,已经有大量临床前和临床研究证实IL-6与多种疾病的发病机制有关,您能从血液科医生的角度来分享一下IL-6与哪些疾病发病相关?
早期人们发现IL-6与感染有关,随着时代的发展,人们逐渐认识到,IL-6属于多效性细胞因子的一种,分泌来源广泛。研究发现,IL-6在特发性多中心型Castleman病(iMCD)的发病机制及临床症状中起关键作用,且有较多证据支持IL-6是iMCD的主要致病因子。IL-6也是CRS的主要介质,可引发血管渗漏、补体系统激活和凝血机制激活等一系列级联反应。
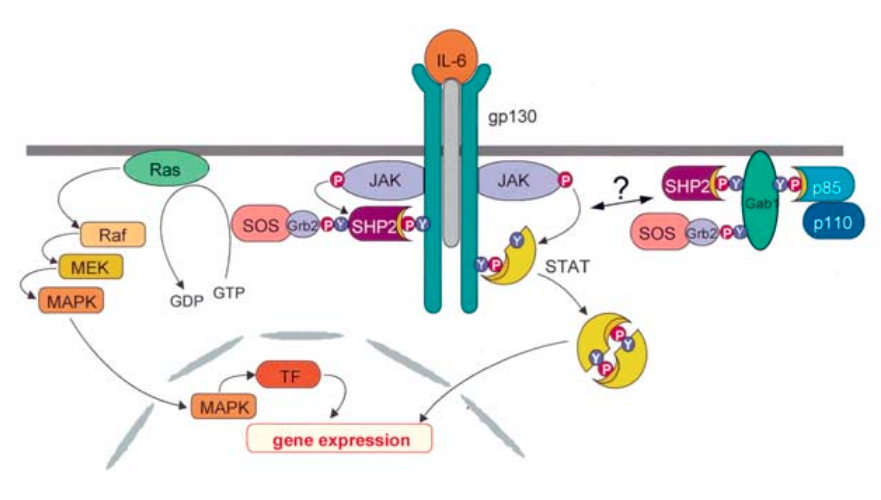
图1 IL-6信号通路转导机制1
除了CD和CRS外,其他血液系统肿瘤如多发性骨髓瘤(MM)中也有IL-6的“身影”。IL-6可通过作用于IL-6受体(IL-6R)参与细胞内JAK1/STAT3信号通路传导,进而影响MM细胞的生存;同时IL-6可以上调B细胞淋巴瘤蛋白-2(BCL-2)、髓样细胞白血病蛋白-1(MCL-1)等抗凋亡蛋白阻止MM细胞凋亡,通过抑制IL-6及其受体下游通路可能会使MM患者受益。
医脉通:近日,司妥昔单抗已经在国内获批用于治疗HIV阴性、HHV-8阴性的MCD成人患者,且获得国内外指南的一致推荐。请您分享一下多项指南都推荐司妥昔单抗作为iMCD的一线治疗首选背后的原因。
司妥昔单抗能够被多项指南推荐作为iMCD一线治疗的首选,主要基于独特的作用机制和扎实的临床研究。
作用机制方面,司妥昔单抗是一款抗IL-6的人鼠嵌合免疫球蛋白G1κ(IgG1κ)型单抗,可以高亲和力地结合人可溶性IL-6,阻断IL-6与IL-6R的结合,抑制其与gp130形成六聚体信号传导复合物,即通过中和IL-6的效应而缓解iMCD的常见症状。
临床研究方面,现有iMCD治疗方案中,司妥昔单抗的循证证据最多,临床研究纳入患者例数最多,且证据级别高,循证基础较其他治疗方案更为扎实。支持司妥昔单抗适应症获批的循证证据是目前iMCD治疗领域唯一一项随机、双盲、对照研究,该研究展示出司妥昔单抗在治疗MCD方面良好的疗效,主要研究终点显示司妥昔单抗治疗组持久应答患者比例显著高于安慰剂组患者(34% vs. 0%,P=0.0012)。

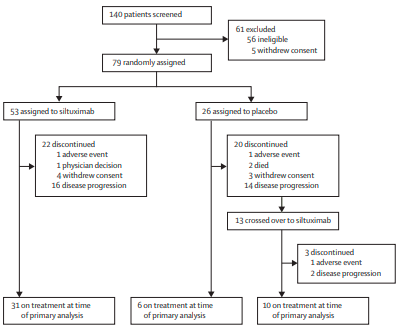
图2 司妥昔单抗治疗MCD随机、双盲、对照研究及设计2
除了疗效,药物的安全性也是临床关注的重点。针对司妥昔单抗的LTSE研究入组了全球26家医学中心的60例患者,该研究旨在评估司妥昔单抗在iMCD患者治疗中的长期安全性和疗效(长达6年)。结果显示:司妥昔单抗长期治疗iMCD的疾病控制率为97%,中位疾病控制时间尚未达到,6年生存率为100%,长期治疗安全性良好。
正是基于司妥昔单抗在Castleman病治疗中的显著疗效和高质量的研究证据,《中国Castleman病诊断与治疗专家共识(2021年版)》3、《中国临床肿瘤学会(CSCO)淋巴瘤诊疗指南(2021年版)》4、NCCN指南5及CDCN共识6等均推荐司妥昔单抗作为iMCD的一线用药。
医脉通:除了CD,IL-6与CRS也密切相关,而血液领域的CAR-T等治疗方法会引起CRS。能否请您阐述一下CAR-T诱导的CRS的特点和发生机制,以及IL-6在其中占有怎样的地位?
CRS本质上是一种由免疫效应细胞过度激活和多种促炎细胞因子(包括IL-1、IL-6、IFN-γ和GM-CSF等)超生理水平诱导的全身性疾病,但其具体的发病机制目前尚不完全清楚。在嵌合抗原受体T细胞(CAR-T)治疗中,CRS是比较常见的不良反应,后续常引起多种器官毒性甚至多器官功能衰竭,严重可导致患者死亡。
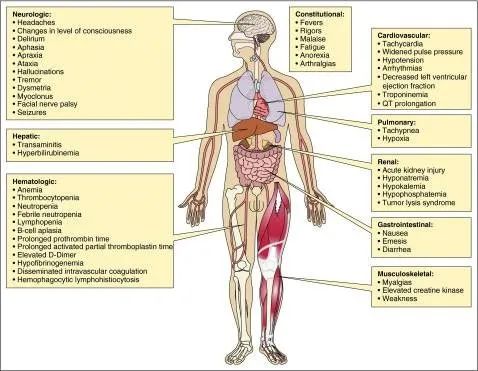
图3 CAR-T治疗后CRS引起多种器官毒性3
IL-6在CAR-T引起的CRS中扮演着重要角色。大量IL-6的升高往往会正反馈促进多种免疫细胞大量激活,也可促进趋化作用。以巨噬细胞为例,大量激活之后,若炎症不加以控制,巨噬细胞会释放多种铁蛋白,进一步导致细胞因子失控。因此治疗CRS的关键在于控制细胞因子的分泌或中和已经分泌的关键细胞因子如IL-6等。
医脉通:能否请您结合自身的临床经验,简要介绍一下CAR-T CRS的管理?
国内外多个指南均包含CAR-T不良反应管理方面的内容,原则一般是包括监测、分级与临床处理。临床实践中,当CRS症状较轻时,一般实行对症处理,如输液、相应退热处理等,但当对症措施无法进一步控制症状时,需采用IL-6的拮抗治疗。后续也可根据患者状况采用广泛免疫抑制剂,如激素等。需注意的是,CRS一般发生在CAR-T治疗后一周,且CRS严重程度与血清IL-6水平和CAR-T细胞水平峰值相关。
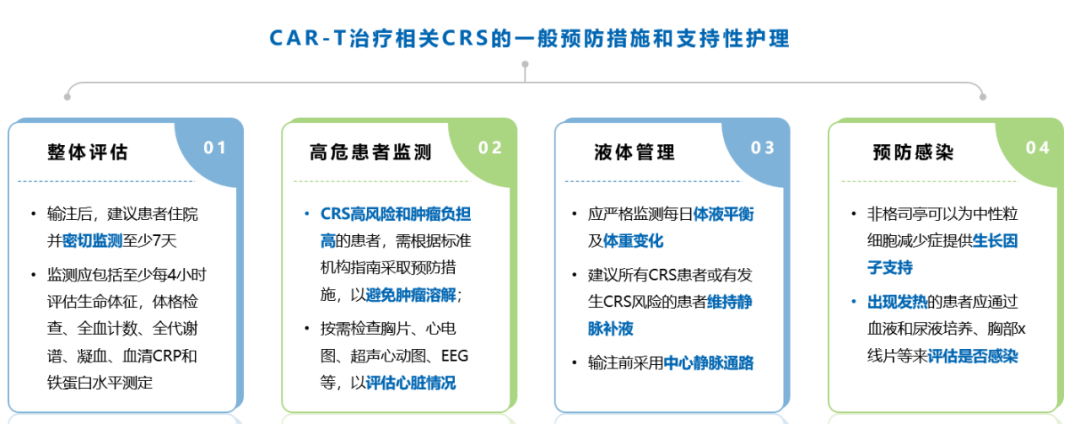
图4 CAR-T治疗相关CRS的一般预防措施和支持性护理
抗IL-6疗法是治疗中重度CRS的关键手段。目前国外临床上常采用IL-6R拮抗剂治疗,但IL-6R拮抗剂可能阻断IL-6R介导的IL-6进入外周组织,导致血清中IL-6水平升高,因此理论上讲,这种IL-6升高的效应可能增加IL-6向中枢神经系统的被动扩散,从而增加神经毒性的风险。国内临床常采用激素治疗,诱发中枢神经系统疾病的比例相对较少。
医脉通:您对司妥昔单抗未来的应用前景有何展望?
截至目前,司妥昔单抗是国内首个也是唯一获批用于治疗iMCD的药物,打破了Castleman病领域无获批药物可用的困境。获批并不意味着司妥昔单抗的应用未来仅仅局限于iMCD,鉴于IL-6生物学活性广泛,与CRS、MM等多种疾病的发病机制相关,作为靶向IL-6的抑制剂,司妥昔单抗或有许多“发挥空间”。目前已经有一些针对司妥昔单抗控制上述疾病的相关临床试验展开。总之,司妥昔单抗作为一种国内刚获批的药物,不仅仅填补了iMCD治疗领域的空白,在其他领域,尤其是CRS方面的应用也很值得期待。
IL-6在CD、CRS、MM等多种疾病发病或治疗过程中扮演着重要角色。临床诊疗过程中,CAR-T治疗诱发的CRS较为常见,IL-6与之密切相关。已有研究发现针对IL-6的抑制剂治疗或可控制相应症状,因此司妥昔单抗的获批为临床保留了一定的“想象空间”,即司妥昔单抗造福iMCD患者的同时,也因其靶向IL-6的特性为其他疾病如CRS等领域治疗提供了可能选择。实践出真知,期待更多临床工作者积极积累临床经验,中国医疗事业添砖加瓦。


周剑峰 教授
-
教授、主任医师、博士生导师
-
华中科技大学同济医学院附属同济医院血液科主任
-
教育部重点实验室“同济医院肿瘤生物医学中心”副主任
-
国家杰出青年基金获得者
-
中华医学会血液分会常务委员、实验诊断学组副组长
-
中国抗癌协会血液肿瘤专业委员会副主任委员、青年委员会主任委员
-
中国基因治疗协会委员
-
中国实验血液学会委员
-
任中华血液学杂志、中国实验血液学杂志、临床血液学杂志、白血病.淋巴瘤、国际输血及血液学杂志等学术杂志编委
-
国家自然科学基金终审评委
-
主要专业方向为白血病、淋巴瘤的分子诊断和个体化治疗
-
在国际期刊如Blood,Nature Genetics, J Exp Med,JNCI 等共发表专业论文70余篇,影响因子> 200分,近5年论文的SCI 总引用一千余次
转载请注明出处。



 相关文章
相关文章



 精彩导读
精彩导读




 热门资讯
热门资讯 关注我们
关注我们


