胃癌作为全球范围内最常见的瘤种之一,备受关注及重视,胃癌诊疗的发展日新月异。由北京市希思科临床肿瘤学研究基金会与CSCO胃癌专家委员会共同主办,杭州东方临床肿瘤研究中心协办的“2021 CSCO胃癌专家委员会学术年会”于2021年12月3-4日在上海隆重召开。在会议上,解放军总医院肿瘤医学部肿瘤内科主任戴广海教授盘点了2021年度胃癌内科治疗的进展。
-
肿瘤学博士,主任医师,教授
-
解放军总医院 肿瘤医学部肿瘤内科 主任
-
CSCO理事
-
胆系肿瘤专委会、胰腺癌专委会 副主任委员
-
智慧医学专委会常委
-
中国研究型医院学会精准医学与肿瘤MDT专业委员会 主任委员
-
中国医师协会结直肠肿瘤专委会MDT专业委员会 主任委员
-
中华医学会肿瘤学分会结直肠肿瘤学组 副主任委员
2021年度胃癌免疫治疗进展
HER2阴性胃癌
ORIENT-16研究
ORIENT-16研究是一项随机双盲、多中心的III期临床试验(NCT03745170),旨在评估信迪利单抗联合化疗(奥沙利铂+卡培他滨)一线治疗不可切除的局部晚期、复发性或转移性胃及胃食管交界处腺癌的有效性和安全性。主要研究终点是总体人群和程序性死亡受体-配体1(PD-L1)阳性人群的总生存期。结果显示,信迪利单抗联合化疗显著降低综合阳性评分(CPS)≥5人群(HR 0.660,95% CI 0.505-0.864,p=0.0023)和总体人群(HR 0.766,95% CI 0.626-0.936,p=0.0090)的死亡风险,达到预设的优效性标准;中位总生存期(mOS)在CPS≥5人群延长5.5个月(18.4月 vs 12.9月),总体人群延长2.9个月(15.2月 vs 12.3月)。OS在预设的所有亚组分析中获益趋势一致。安全性特征与既往报道的信迪利单抗相关临床研究结果一致,无新的安全性信号。
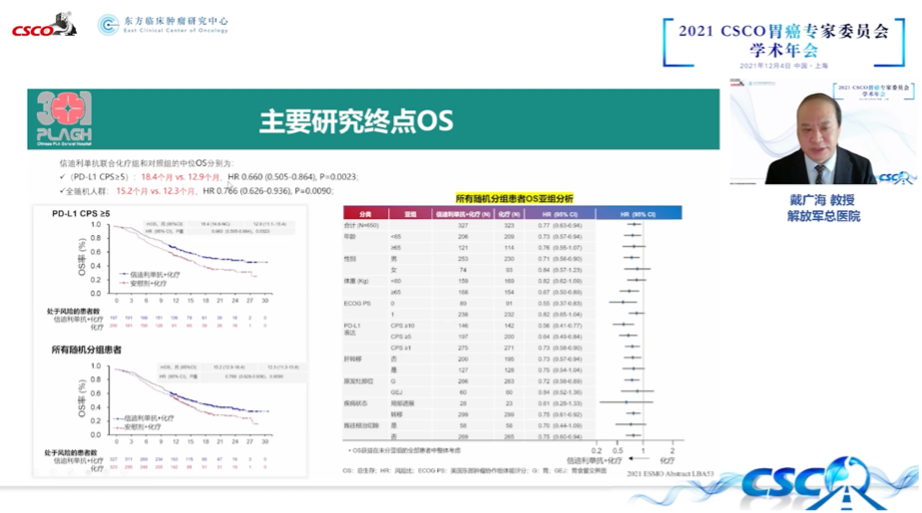
CheckMate-649研究
CheckMate-649研究是一项全球多中心、开放标签、III期临床研究。其研究结果表明,纳武利尤单抗+化疗继续显示生存获益,但纳武利尤单抗+伊匹木单抗未显示优势;在CPS≥5和所有随机人群中,纳武利尤单抗+伊匹木单抗对比化疗OS均未显示出优势,但双免缓解持续时间(DOR)均显著延长。
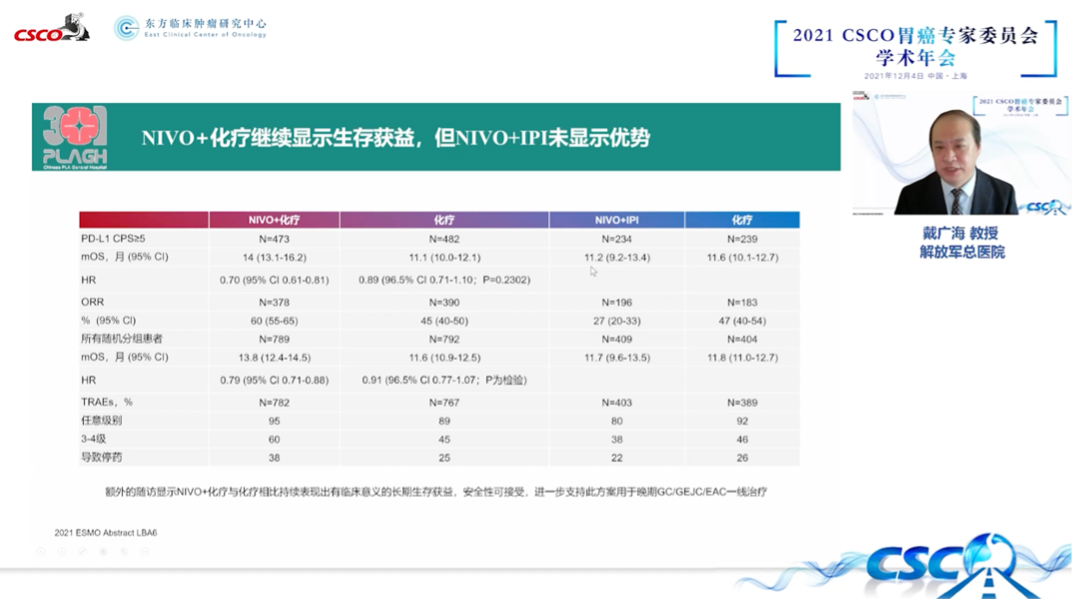
面临问题及未来探索
目前已完成的研究有CheckMate-649、ATTRACTION-4、KEYNOTE-062、JAVELIN GASTRIC 100、ORIENT-16研究,正在进行中的研究有SHR-1210-III-310、KEYNOTE-859、E7080/MK-7902、CIBI308E301、BGB-A317-305、NCT03802591研究。
戴广海教授表示,在研究中,随着PD-L1的选择增加,免疫治疗+化疗获益趋势更加明显,意向治疗分析人群的阳性是否有PD-L1驱动还不得而知,需要参考CheckMate-649以及ORIENT-16研究中CPS<1和CPS<5的数据,并且检测的标准化亟需确立。
对于一些其他治疗模式的探索研究,初步结果提示卡瑞利珠单抗+化疗序贯卡瑞利珠单抗+阿帕替尼一线治疗晚期胃及胃食管交界处腺癌,具有良好的抗肿瘤活性和生存期,安全性可控。此外,PLATFORM研究是一项前瞻性、开放标签、多中心II期研究,评估一线化疗后度伐利尤单抗维持治疗用于食管、胃及胃食管交界处腺癌的疗效,其研究结果表示,观察组和度伐利尤单抗维持治疗组的中位无进展生存期(PFS)分别为3.2个月和4.7个月,差异没有统计学意义。两组的中位OS分别为11.4个月和11.3个月,差异也没有统计学意义。在3个月时观察组无患者缓解,度伐利尤单抗维持治疗组客观缓解率(ORR)为6%,其中完全缓解率(CR)为2%,部分缓解率(PR)为4%。对于免疫单药的价值方面,KEYNOTE-062研究表示,无论是PD-L1 CPS≥1还是CPS≥10的患者,帕博利珠单抗联合化疗对比单纯化疗,并未取得更优的OS,但是对于CPS≥10的患者,可以考虑帕博利珠单抗单药治疗,特别是化疗耐受性差的患者。
KEYNOTE-811研究
KEYNOTE-811研究是一项随机、安慰剂对照、双盲、Ⅲ期临床试验,旨在对比帕博利珠单抗联合一线标准治疗和一线标准治疗在HER2+转移性胃及胃食管交界处腺癌的临床疗效,其研究结果提示,帕博利珠单抗联合标准一线治疗方案(SOC)组的ORR(95%CI)为74.4%(66.2-81.6),安慰剂联用SOC组的ORR为51.9%(43.0-60.7);两组的CR率分别为11.3%和3.1%,DCR分别为96.2%和89.3%。帕博利珠单抗联用SOC组的中位(范围)DOR为10.6个月(范围1.1-16.5),安慰剂联用SOC组为9.5个月(范围1.4-15.4)。基于该研究结果,帕博利珠单抗获美国食品药品监督管理局(FDA)批准的HER2阳性晚期胃癌一线适应症。
INTEGA研究
INTEGA研究为伊匹木单抗或FOLFOX化疗方案联合纳武利尤单抗、曲妥珠单抗在既往未接受过系统治疗的HER2阳性晚期胃食管交界处腺癌患者的随机、双盲、安慰剂对照、单中心II期研究。其研究结果表明去化疗的双免疫联合曲妥珠单抗治疗没有增加HER2阳性晚期胃癌患者OS、PFS获益。
2021年度胃癌靶向治疗进展
HER2靶点
Zanidatamab(ZW25)
ZWI-ZW25-201(NCT03929666)是一项正在进行的多中心、全球、Ⅱ期的开放标签研究,旨在评估ZW25+标准一线联合化疗方案在局部晚期、无法切除或转移性的HER2表达的胃食管癌受试者(包括胃食管腺癌)中的安全性、耐受性和抗肿瘤活性。其研究结果表明,在安全性方面,36例胃食管腺癌患者中,19例(53%)继续接受研究治疗,12例(33%)因疾病进展而停止治疗,4例(11%)因临床进展而停止治疗,1例(3%)由医生决定停止治疗;此外,所有治疗方案的总体ORR为75%,中位DOR为16.4个月,中位PFS为12个月。
抗体偶联药T-DXd(DS-8201)
DESTINY-Gastric01研究是一项多中心、开放标签、随机、II期研究,共入组187例先前接受过至少2种方案治疗后疾病进展的HER2阳性晚期胃及胃食管交界处腺癌患者,其研究结果提示,DS-8201组的ORR和OS显著优于化疗组:两组的ORR分别为51%和14% (P<0.001),中位OS分别为12.5个月和8.4个月(P=0.01),中位PFS为5.6个月和3.5个月。
DESTINY-Gastric02是评估T-DXd治疗HER2+胃及胃食管交界处腺癌患者的开放标签、多中心的Ⅱ期试验。该研究共纳入了79例患者,每例患者以6.4mg/kg Q3W的标准用药,这些患者先前接受过2种或多种方案(包括5-FU、含铂化疗、曲妥珠单抗)。截至2021年4月9日,研究达到了主要终点和关键次要终点:在79例可评估患者中,通过独立中央审查(ICR)评估的ORR为38%,疾病控制率(DCR)可达81%。中位PFS为5.5个月,DOR为8.1个月。
FGFR2b靶点
FIGHT研究是Bemarituzumab联合mFOLFOX6对比安慰剂联合mFOLFOX6方案在一线治疗FGFR2b+、晚期胃及胃食管交界处腺癌的随机、双盲、安慰剂对照、II期临床试验,其研究结果提示,FGFR2b+过表达程度与Bemarituzumab疗效呈正相关,Bemarituzumab显著延长了患者中位OS5.7个月。
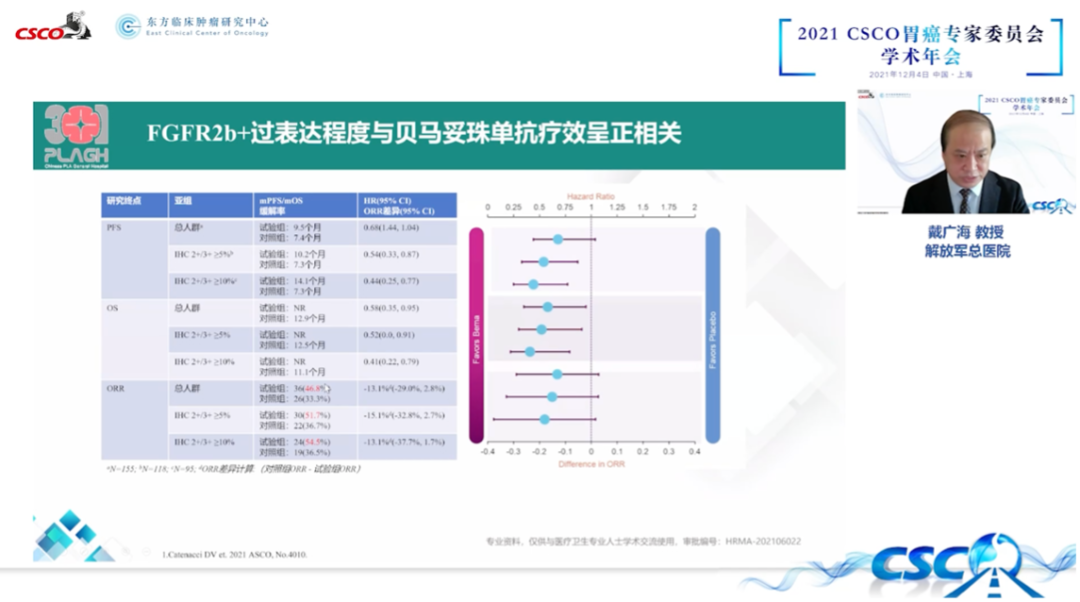
小结
转载请注明出处。

 相关文章
相关文章

 精彩导读
精彩导读




 热门资讯
热门资讯 关注我们
关注我们


